Hafızanın Yeni Tehlike Sensörü: Grafen Alan Etkili Transistör
Sena Uslu
Bilincimiz varlığımızın farkındalığını oluşturarak çevremizle bağlantıda kalmamızı sağlar. Hafıza kaybı ve bilinç bozukluğu gibi durumlarda kendimizle ve dünyayla olan ilişkimiz kopmaktadır. Nörodejeneratif hastalıklardan olan Alzheimer ve Parkinson, beyinde yarattığı yıkıcı etkilerden ve klinikte oluşturduğu dramatik tablolardan ötürü erken teşhisi son derece önemli hastalıklardandır. Alzheimer, nöronlarda tau ve amiloid beta proteinlerinin birikmesiyle karakterizedir. Parkinson ise dopaminerjik nöronlarda alfa sinüklein proteininin birikmesi sonucu nöron kaybıyla seyreden bir hastalıktır. Günümüzde bu hastalıkların tanısı klinik semptomlarla konulmaktadır. Ancak semptomların ortaya çıktığı dönemde protein birikimi artık geri dönülmez bir hal almıştır. Bu nedenle birikimin daha en başından, çeşitli biyolojik sıvı örneklerinden izole edilen amiloid beta, tau ve alfa sinüklein proteinlerinin ölçülmesinin hastalığın erken tanısı ve tedavisi için umut verici olduğu düşünülmüştür.
Günümüzde nörodejeneratif hastalıklarda biriken proteinleri hedef alan birçok çalışma mevcuttur. Bu çalışmada [PNAS 2023 Nov 21;120(47):e2311565120] ise kan, tükürük, beyin-omurilik sıvısında “femtomolar” (10 -15 molar) konsantrasyondaki amiloid beta, tau ve alfa sinüklein proteinlerinin Grafen Alan Etkili Transistör (GAET) [Graphene Field Effect Transistor] ile tespit edilerek erken tanıya gidilmesi planlanmıştır. Biyolojik sıvı örneğinin damlatıldığı çipin içeriğinde bulunan GAET, hasta başında ve evde uygulanabilecek kullanışlı ve hızlı bir yöntemdir. GAET’in diğer alan etkili transistörlerden önemli bir farkı iki boyutlu karbon tabakasından oluşmasıdır. Bu özellik GAET’in iletkenliğini arttırarak daha küçük uyaranlara daha kuvvetli sinyal oluşturmasını sağlamaktadır. Dolayısıyla GFET’in çok düşük konsantrasyonlardaki hedef proteinleri tespit ederek hastalıkların erken tanısına olanak sağlayacağı belirtilmiştir.
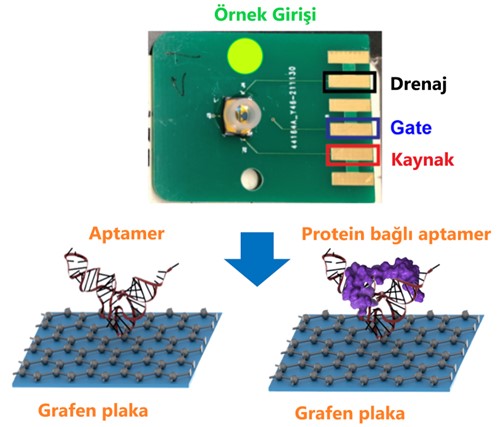
GAET’in sinyal oluşturma mekanizmasında 3 elektrot ön plandadır. İlk iki elektrot kaynak ve drenaj elektrotlarıdır. İkisinin arasında grafen tabaka bulunur ve üzerinden akım geçmektedir. Diğeri ise kanaldaki akım değişikliği sonucu oluşan voltaj farkı (delta Vg) sayesinde sinyal veren “gate” elektrotudur. Akım değişikliği hedef proteinlerin grafendeki spesifik aptamerlere bağlanmasıyla oluşmaktadır. Voltaj değişikliğinin derecesine göre hedef proteinlerin konsantrasyonu ölçülmüştür. (Görsel 1)
Çalışmada amiloid beta, tau ve alfa sinüklein proteinlerinin algılanılabilir en düşük konsantrasyonları, delta Vg değerlerine göre belirlenmiştir. Sonrasında her bir proteine özgül olan aptamerlerin spesifikliği ölçülmüştür. Aptamerlerin; amiloid beta, tau ve alfa sinüklein proteinlerinin üç boyutlu yapılarını ve izoformlarını ayırt edebildiği gösterilmiştir. Böylece aralarında çapraz reaksiyon olmadığı, sadece spesifik oldukları proteinlere duyarlı oldukları bilgisi elde edilmiştir. Bu proteinlerin sentetik formlarından elde edilen bilgiler Alzheimer hastası beyin dokularının otopsisinden izole edilen proteinlerle yapılan çalışmalarla doğrulanmıştır. Ayrıca erken evre Alzheimer hastalarındaki ve sağlıklı insanlardaki bu protein değerlerinin GAET’in algılayabildiği konsantrasyon aralığında olduğu gösterilmiştir. Ancak tespit edilecek proteinin boyutu, yükü gibi özelliklerin biyosensörün duyarlılığında bozulmalara sebep olabildiği belirtilmiştir. Örneğin tau proteininin büyük olması sinyalde yanlış pozitifliklere, pozitif yüklü olması ise GAET’in negatif yüklü moleküllere daha duyarlı olması nedeniyle daha düşük sinyal oluşturmasına neden olmuştur. Bu tür kısıtlamaların giderilmesi için izoforma spesifik aptamerlerin üretimi ve biyosıvılardan amiloid beta, tau ve alfa sinüklein tespiti üzerinde çalışmalar devam etmektedir.
İçerdiği grafen ile muadillerinden daha hassas ölçümler yapabilen GAET’in Alzheimer ve Parkinson gibi tanısı ancak geç dönemde konan ve bu nedenle tedavi başarısının düşük olduğu nörodejeneratif hastalıkların hızlı ve erken teşhisinde umut verici olduğu belirtilmektedir. Beyinde birikeceği bölgeye doğru giden proteinlerin biyolojik sıvı içerisinde daha ihmal edilebilir konsantrasyondayken tespit edilmesiyle avantaj sağlayacağı düşünülmektedir. Bu çalışmaların vesilesiyle hastaların beyinlerinde birikenler geçmişinin üzerine çizgi çeken proteinler değil, her daim hatırlayacakları anıları olacaktır.

